佐妥昔单抗(zolbetuximab)是一种针对CLDN18.2靶点的单克隆抗体药物,用于治疗CLDN18.2阳性的晚期胃及胃食管结合部腺癌。由于该药是近年来新获批的靶向治疗药物,许多患者和医生关注其正式上市时间。本文将从适应症、原研药生产厂家、上市情况、价格情况及购买注意事项等方面进行介绍。
适应症
佐妥昔单抗联合含氟嘧啶和铂类的化疗方案,适用于局部晚期不可切除或转移性人表皮生长因子受体2(HER2)阴性胃或胃食管结合部腺癌成年患者的一线治疗。患者肿瘤需经FDA批准的检测方法确认为CLDN18.2阳性。
原研药生产厂家
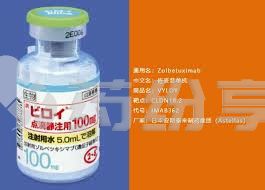
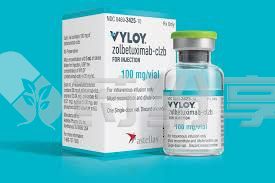
佐妥昔单抗的原研药由德国安斯泰来制药(Astellas Pharma)研发生产,该药是全球首个获批上市的靶向CLDN18.2的单克隆抗体药物。
![images [最大宽度 320 最大高度 240] 2026051203121618517](/upload/ueditor/image/20260512/2026051203121618517.jpg)
上市情况
1.海外上市时间:佐妥昔单抗于2024年获得美国食品药品监督管理局(FDA)批准上市,用于CLDN18.2阳性的晚期胃及胃食管结合部腺癌的一线治疗。
2.中国上市时间:该药目前已在中国大陆正式获批上市。国内上市规格为100mg的原研版本。需要注意的是,该药目前暂时未纳入国家医保目录。
价格情况
佐妥昔单抗目前国内的原研药已上市,目前暂时没有纳入国内医保报销项目,据了解,国内上市的规格为100mg的原研版本价格大概需要不到6000元。此外,目前市面上还未出现佐妥昔单抗的仿制药。
购买注意事项
1.佐妥昔单抗为静脉输注用药,需在医疗机构内由专业人员操作。推荐剂量为首次800mg/m²,后续每3周600mg/m²或每2周400mg/m²。
2.用药前必须通过FDA批准的检测方法确认肿瘤CLDN18.2阳性,且患者需为HER2阴性胃或胃食管结合部腺癌。
3.每次输注前需预先使用止吐药物(如NK-1受体阻滞剂和/或5-HT3受体阻滞剂),以预防恶心和呕吐。如果佐妥昔单抗与化疗同一天给药,需先输注佐妥昔单抗。
4.患者应凭正规医疗机构处方购药,确保药品来源可靠。治疗期间需定期监测不良反应。
佐妥昔单抗于2024年在海外获批上市,目前已在中国大陆正式上市,国内规格100mg每盒价格不到6000元,尚未纳入医保。该药适用于CLDN18.2阳性的HER2阴性晚期胃及胃食管结合部腺癌的一线治疗,需在医生指导下与化疗联合使用,并注意输注前的止吐预处理。
关键词标签:佐妥昔单抗、zolbetuximab、VYLOY、CLDN18.2、胃癌、胃食管结合部腺癌、HER2阴性、安斯泰来、上市时间、国内上市、价格情况、购买注意事项
参考资料:https://www.drugs.com/vyloy.html


![下载 (2) [最大宽度 320 最大高度 240] 2026051202512656475](/upload/ueditor/image/20260512/2026051202512656475.jpg)
![Zolbetuximab [最大宽度 320 最大高度 240] 2026051202263091858](/upload/ueditor/image/20260512/2026051202263091858.jpg)
![adlumiz [最大宽度 320 最大高度 240] 2026043002133950294](/upload/ueditor/image/20260430/2026043002133950294.jpg)

![42e4663954bd4b2f81a148aededb908d [最大宽度 320 最大高度 240] 2026043002002379721](/upload/ueditor/image/20260430/2026043002002379721.jpg)
![images [最大宽度 320 最大高度 240] 2026042111564257066](/upload/ueditor/image/20260421/2026042111564257066.jpg)