莫洛替尼(Momelotinib)是一种创新型口服JAK1/JAK2及ACVR1抑制剂,主要用于治疗中高危骨髓纤维化(MF)成人患者,尤其适合伴有贫血症状的患者。其通过抑制异常活化的JAK-STAT信号通路,减轻骨髓炎症并抑制恶性克隆增殖,同时通过调节铁代谢改善贫血,减少输血依赖。作为靶向治疗药物,莫洛替尼的储存条件直接影响其稳定性和疗效,患者需严格遵循规范保存。
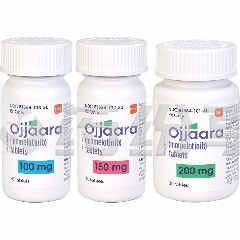
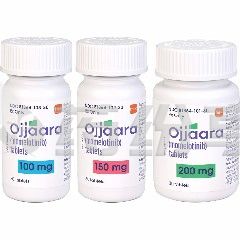
莫洛替尼的储存核心要求是控制温湿度、避光防潮。药物应保存在原始包装瓶中,瓶内配备的干燥剂包可有效吸收潮气,防止药片受潮变质,因此切勿丢弃干燥剂。储存温度需保持在20℃至25℃的室温环境,允许短期波动至15℃至30℃,但需避免极端温度。例如,夏季高温时应远离暖气、阳光直射的窗台或汽车内,冬季寒冷时则需避免放置在暖气旁或室外。湿度控制同样关键,浴室、厨房等潮湿环境可能加速药物分解,建议存放在干燥、阴凉的柜子或抽屉中。
![5b508f59267744b38622be7345d9d216-Ojjaara_all-str [最大宽度 320 最大高度 240] 2026050811265329996](/upload/ueditor/image/20260508/2026050811265329996.jpg)
日常使用中,每次取药后需立即拧紧瓶盖,减少药物与空气的接触时间。若药物不慎掉落或包装破损,可能因污染或受潮影响药效,建议咨询药师后处理。长期储存时,无需将药物放入冰箱,但需定期检查药片状态,若出现变色、粘连或异味,应立即停用并联系医生。
总之,莫洛替尼的正确保存需围绕“避光、密封、控温”展开,严格遵循原包装储存、控制温湿度波动、避免潮湿环境等原则,可最大限度保障药物稳定性,为治疗提供安全支持。
关键词标签:莫洛替尼、储存条件、室温保存、避光防潮、干燥剂、骨髓纤维化
参考资料:https://www.ema.europa.eu/en/medicines/human/EPAR/omjjara


![images [最大宽度 320 最大高度 240] 2026050811273107174](/upload/ueditor/image/20260508/2026050811273107174.jpg)

![下载 [最大宽度 320 最大高度 240] 2026050811281143311](/upload/ueditor/image/20260508/2026050811281143311.jpg)

![下载 [最大宽度 320 最大高度 240] 2026050611424491837](/upload/ueditor/image/20260506/2026050611424491837.jpg)
![images [最大宽度 320 最大高度 240] 2026050611414833162](/upload/ueditor/image/20260506/2026050611414833162.jpg)
![5b508f59267744b38622be7345d9d216-Ojjaara_all-str [最大宽度 320 最大高度 240] 2026050611393409926](/upload/ueditor/image/20260506/2026050611393409926.jpg)